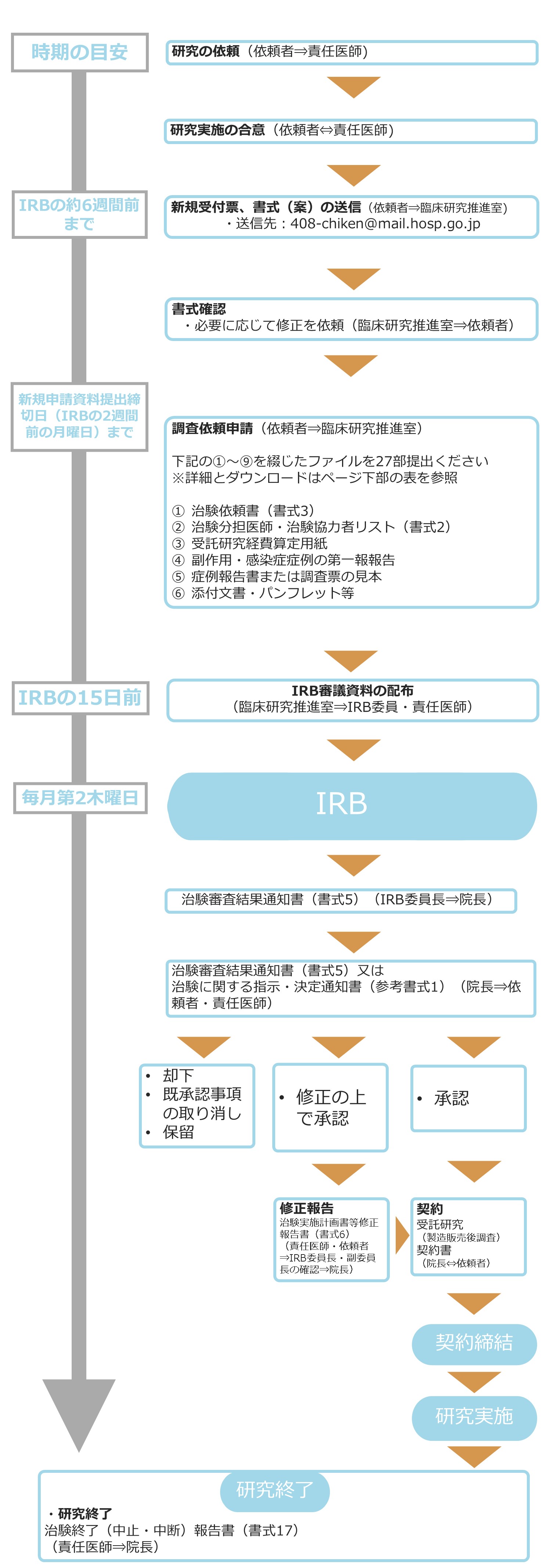
その他(副作用等) 新規申請手続きの流れ
その他(副作用等) 新規申請時提出書式一覧
新規申請時
|
書式No |
様式名 |
副作用・感染症症例調査 |
体外診断用医薬品 |
その他 |
|---|---|---|---|---|
| 書式2 | 治験分担医師・治験協力者 リスト | |||
| 書式3 | 治験依頼書 | |||
| 様式1-6 | 受託研究(治験等以外)契約書 | |||
| 様式1-2 | 受託研究(製造販売後調査)契約書 | |||
| 別紙基準3 | 受託研究経費算定用紙 3.体外診断用医薬品に係る経費算出基準 |
|||
| 別紙基準4 | 受託研究経費算定用紙 4.市販後調査に係る経費算出基準 (1)使用成績調査・特定使用成績調査 |
|||
| 別紙基準6 | 受託研究経費算定用紙 4.製造販売後調査に係る経費算出基準 (3)副作用・感染症報告経費 |
|||
| 別紙基準7 | 受託研究経費算定用紙 5.その他受託研究に係る経費算出基準 |
|||
| 別表3 | 臨床性能試験研究経費ポイント算出表 | |||
| 別表4 | 相関及び性能試験研究経費ポイント算出表 | |||
| 研究実施計画書(合意が確認できるもの又は責任医師用の合意書) |
○ |
○ |
||
| 説明・同意文書の案 |
△ |
|||
| 副作用・感染症症例の第一報報告 |
○ |
|||
| 症例報告書の見本 |
○ |
○ |
○ |
|
| 添付文書・パンフレット等 |
○ |
○ |
○ |
◎はどちらか該当するもの
△は必要な場合もある
その他(副作用等) 実施中の手続き
同意説明文書改訂
実施要綱等の改訂、契約期間・症例数等の変更
|
書式No. |
書式名 |
副作用・感染症症例調査 |
体外診断用医薬品 |
その他 |
|---|---|---|---|---|
| 書式10 | 治験に関する変更申請書 | |||
| 様式1-4 | 契約内容変更に関する覚書(二者契約用) | |||
| 様式1-5 | 契約内容変更に関する覚書(三者契約用) | |||
| 別表3 | 臨床性能試験研究経費ポイント算出表 | |||
| 別表4 | 相関及び性能試験研究経費ポイント算出表 | |||
| 別紙基準3 | 受託研究経費算定用紙 3.体外診断用医薬品に係る経費算出基準 |
|||
| 別紙基準7 | 受託研究経費算定用紙 5.その他受託研究に係る経費算出基準 |
|||
| 変更・改訂後の資料等 |
○ |
○ |
注1:●は研究経費の変更が伴う場合必要
注2:◎、( )はどちらか該当するもの
注3:別表及び別紙基準は変更前後を提出
分担医師の追加
安全性情報等に関する報告
治験実施計画書からの逸脱に関する報告
▲緊急の危険回避のための逸脱










